運動失調(ふらつき、登れていた段差も登らなくなった)の主訴で来院。
症例紹介 CASE
症例紹介 CASE
起源不明髄膜脳炎(MUO)とは?
MUOは、犬の中枢神経(脳・髄膜、ときに脊髄)に生じる炎症性疾患のうち、臨床的に感染性・腫瘍性・代謝性などの明確な原因が特定できず、免疫介在性の炎症が疑われる症例群をまとめた包括的な呼称です。臨床現場では、組織学的確定が得られない状況で用いられることが多く、近年はMUOとほぼ同義に MUE(meningoencephalomyelitis of unknown etiology) という用語が併用されることもあります。MUOは単一疾患というより、「病理学的に複数の病型が含まれ得る“枠組み”」として理解しておくことが重要です。
【病理学的に想定される主な病型】
MUOの代表的な病理学的サブタイプとして、一般に GME(肉芽腫性髄膜脳炎)、NME(壊死性髄膜脳炎)、NLE(壊死性白質脳炎) が挙げられます。これらは炎症細胞浸潤のパターンや壊死の有無・分布などが異なるとされ、犬種素因を示唆する議論もあります。一方で、臨床では病理確定に至らないことが多いため、個々の症例がどの病型に近いかは「推定」に留まる場合が少なくありません。
【どんな犬に起こりやすいか(疫学の概観)】
MUOは小型犬での報告が多く、若齢〜中年齢で発症するケースがよくみられます。ただし、あくまで「多い傾向」であり、犬種や年齢を限定して起こる疾患ではありません。臨床的には、症状の出方(急性〜亜急性の進行、再燃の有無など)や神経学的な病変分布が症例ごとに大きく異なることが、MUOの特徴の一つです。
【何が起きていると考えられているか(病態の考え方)】
MUOは、現在の理解では「原因不明だが免疫反応が関与する中枢神経炎症」と捉えられることが多く、炎症の結果として脳実質・髄膜(場合により脊髄)に浮腫、組織障害、神経機能の破綻が生じます。感染性病原体が直接原因であることを支持する決定的根拠は確立していない一方、原因探索としてメタゲノム解析など新しいアプローチも試みられており、MUOという枠組み自体が今後さらに精緻化される可能性があります。
【臨床的に見られやすい症候(診断論は除外)】
MUOの症候は、病変の主座(前脳、脳幹、小脳など)と分布(局在性か多発性か)に強く依存します。臨床では、けいれん、意識レベルの低下、旋回、運動失調、姿勢反応低下、脳神経症状などが問題となり得ます。経過も多彩で、急速に悪化する例がある一方、一定期間の安定と再燃を繰り返す例もあります。
【予後について】
MUOの予後は一言で断定しにくく、短期に死亡する重症例が一定数存在する一方で、長期生存例も少なくないという「分散の大きい疾患」として説明するのが適切です。数値は研究の症例選択や重症度、追跡期間、治療内容の違いで変動し得る点に注意が必要です。
まず短期予後について、近年の総説・研究では「診断後1週間以内に25–33%が死亡する」と記載されています。また、1週間生存に焦点を当てた回顧研究(116例)では、26%が7日以内に死亡し、提示時の意識低下やけいれんなどが不良転帰と関連していました。
このことは、MUOが「治療開始後も初期に急変し得る疾患」であり、初期の重症度が転帰に影響しやすいことを示唆します。
中期(数か月)では、より大規模なデータとして、447例の回顧研究で退院まで生存が82%、6か月時点で生存が63.5%と報告されています。さらに、6か月生存例のうち36%で神経学的後遺症が残存したとされ、単に生存だけでなく機能予後(どの程度回復するか)も重要な説明要素になります。
長期予後については研究により幅がありますが、たとえば別の回顧研究では生存期間中央値540日、1年以上生存が約55.56%、5年以上生存が約10.55%と報告されています。つまり、MUOは「致死的になり得る」一方で、「一定割合で年単位の生存が見込める」疾患でもあります。
なお、MUOの一部であるGMEに関しては古典的研究で、生存期間が1日から1,215日超まで幅広く、局在性か多発性かといった臨床像の違いで生存が異なり得ることが示されています。この点は、MUO全体でも「病変分布や提示時の神経学的重症度が予後に影響し得る」という一般的な理解と整合します。
症例紹介
神経学的検査では、姿勢反応や脊髄反射に明らかな異常所見は認められなかった。
歩様検査では、点頭歩行および後肢のふらつきを認めた。
初診から4か月後に重積発作で来院されたため、MRI検査を実施。
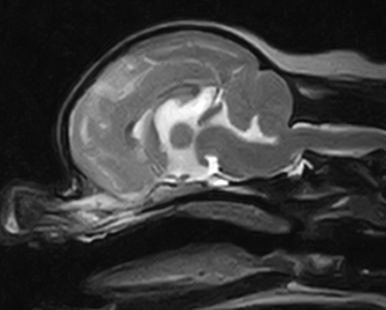
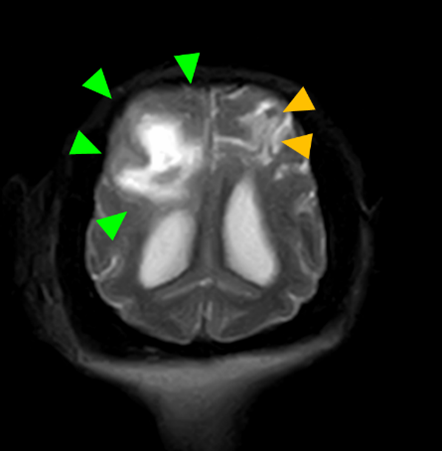
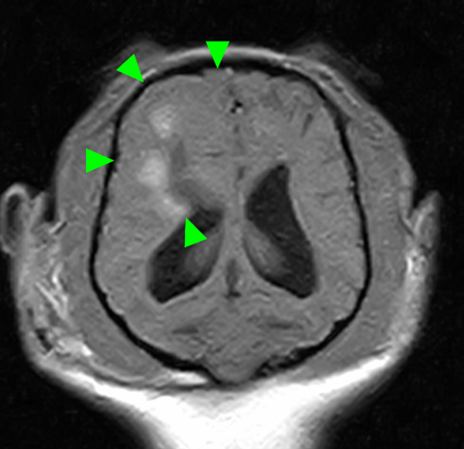
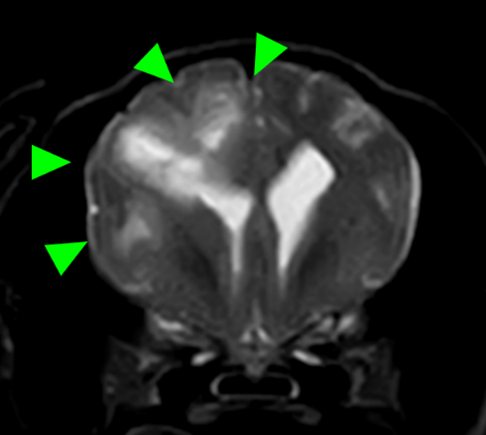
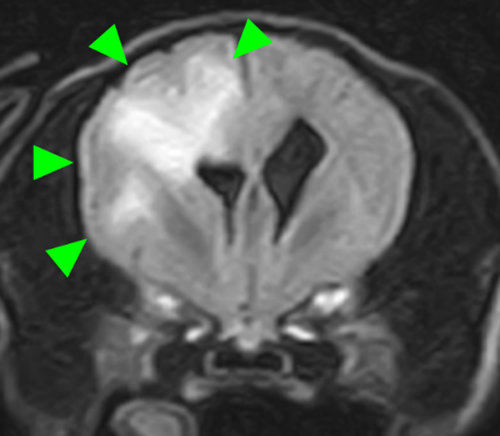
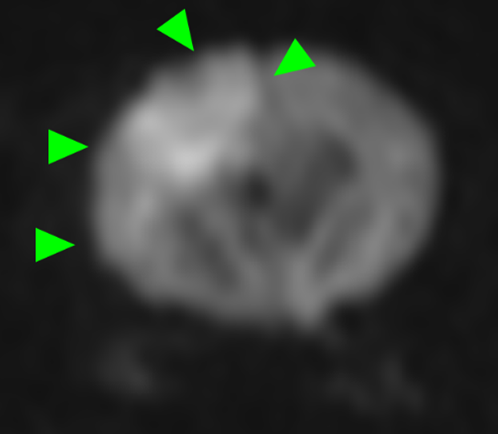
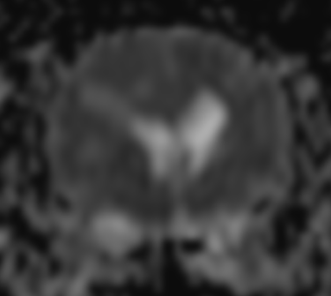
MRI検査:
右前頭葉にT2 強調画像/FLAIR 画像で高信号、T1 強調画像で一部低信号を示し、辺縁部で一部造影増強を示すびまん性の所見を認めた。この所見は、DWI 画像で高信号、ADC-map で大半が等~低信号を示していた。また左側前頭葉にも同様の信号所見を示す微小病変を認めた。
診断と治療
『MUO治療の基本方針』
MUOの治療は、原因病原体を直接叩くというより、中枢神経で起きている免疫介在性炎症を抑え、神経機能の破綻(けいれん、意識障害、歩行障害など)を最小化し、再燃を防ぐことが中心になります。したがって治療の“軸”は、(1)免疫抑制療法(炎症の鎮静化)と、(2)症候(特にけいれんや脳圧亢進が疑われる状態)への支持療法の二本立てです。近年のレビューでも、MUO治療の中心が免疫抑制である点は一貫して強調されています。
1) 免疫抑制療法:ステロイドを“核”に、もう1剤を組み合わせるのが主流
実臨床では、副腎皮質ステロイド(プレドニゾロン/プレドニゾン等)を基幹薬として開始し、そこに第2の免疫抑制薬(例:シタラビン、シクロスポリン、ミコフェノール酸モフェチル等)を併用して、ステロイドを漸減しながら長期維持を図る、という戦略が広く採られています。近年の総説では、文献全体として「ステロイド+シタラビン」または「ステロイド+シクロスポリン」を支持する報告が多い、という整理がなされています。
ただし重要なのは、“どれが絶対に最良”という単一プロトコルは確立していない点です。比較研究でも、プロトコル間で短期悪化率や生存が明確に一方向へ優越するとは限らない、という結論が示されています。
したがって現実的には、神経学的重症度、併発疾患、飼い主の通院許容度(点滴・入院の可否)、副作用リスク、費用などを踏まえて「その犬に最も運用しやすい組み合わせ」を選ぶ、という考え方になります。
2) 代表的な併用薬(第2免疫抑制薬)の考え方
ここからは、MUOでよく選択される併用薬の“位置づけ”を文章で説明します。
シタラビン(cytarabine / cytosine arabinoside)
シタラビンは、神経炎症疾患で古くから用いられてきた薬剤で、投与方法としては皮下反復投与やCRI(持続静注)など複数の運用があります。標準的な皮下投与スケジュールとして、薬物動態研究で「50 mg/m²を12時間ごとに2日間(計4回)」が“標準プロトコル”として扱われています。
一方で、臨床アウトカムに関しては、静注シタラビンを含むプロトコルが短期生存を必ずしも改善しない、という報告もあり、重症度や全体設計の中で位置づける必要があります。
シクロスポリン(cyclosporine)
シクロスポリンはT細胞を中心とした免疫反応を抑える薬剤で、ステロイドの減量を後押しする目的で併用されます。近年、プレドニゾロン単独よりも、シクロスポリン併用の方が再発(relapse)が少ないと報告した研究も出ています。
ただし個体差があり、消化器症状や歯肉増殖、多毛などの副作用が問題になることもあるため、長期運用では副作用管理とモニタリングが重要になります(古典的報告でも副作用が整理されています)。
ミコフェノール酸モフェチル(MMF: mycophenolate mofetil)
MMFは、近年MUOでの使用報告が蓄積している併用薬の一つです。回顧研究では、10 mg/kgを12時間ごとの免疫抑制として用いた経験が報告され、「安全に使用できた」という結論が示されています。
また別の報告では、初期投与量が10–20 mg/kgを12時間ごとの範囲で運用され、寛解後に減量していく実際の流れも記載されています。
注意点として、MMFは下痢など消化器副作用が問題になり得るため、導入初期の観察と用量調整が現実的に重要です(この点は治療レビューでも繰り返し議論されています)。
3) “寛解導入”と“維持”、そして漸減の考え方
MUO治療では、最初の数週間〜1–2か月で炎症を強く抑えて症状を落ち着かせ(寛解導入)、その後は再燃を起こさない最小限の免疫抑制へ落としていく(維持・漸減)という設計になります。ところが、ステロイドの「いつ・どれくらいの速さで減らすべきか」は、文献上も“最適解”が確立しておらず、臨床医の判断に依存する、という整理がされています。
4) 症候に対する治療(支持療法)の役割
MUOは炎症そのものだけでなく、炎症の結果として出現する症候(けいれん、意識障害、重度の運動失調など)が生命予後・生活の質を左右します。そのため実際の治療は、免疫抑制と並行して、抗てんかん薬の併用、必要に応じた入院管理(輸液、栄養、体温・血糖管理など)、さらに重症例では脳圧亢進が疑われる状況への対応といった支持療法が組み合わされます。レビューでも、けいれんなどの随伴症状に対する補助治療がしばしば必要である点が述べられています。
5) 治療中のモニタリングと合併症対策
MUOの治療は「薬を出して終わり」ではなく、免疫抑制が強いほど感染症、消化器障害、肝障害、骨髄抑制などの合併症リスクが上がります。したがって、治療中は一般に、血液検査(CBC・生化学)を中心とした定期モニタリング、臨床症状の小さな変化(元気・食欲・便性状・呼吸状態など)の早期把握が重要になります。
また、長期の高用量ステロイドや多剤併用では、まれに日和見感染が問題になる可能性があるため、発熱・咳・呼吸困難などが出た場合は「様子見」ではなく早期受診が望ましい、という注意喚起は実務上有用です(人医療ではTMP-SMXによるPneumocystis肺炎予防が標準的に議論されており、“免疫抑制=感染リスク”という構図の説明に説得力があります)。
6) 再発(再燃)時の考え方
MUOは、いったん落ち着いても再燃することがあります。再燃時は、免疫抑制の強度を一時的に上げる、併用薬の変更・追加を検討する、といった“戦略の再設計”が必要になることが多く、近年の研究でも再発は重要な臨床テーマとして扱われています。
再発頻度を下げる可能性が示された併用(例:シクロスポリン+プレドニゾロン)も報告されているため、再燃を繰り返す症例では「薬の組み合わせの見直し」が現実的な打ち手になります。
その後の経過(オペ後)
本症例では、プレドニゾロン+シクロスポリンの併用によって発作を含めた神経症状は認められず、元気に過ごしています。
